VERSO LO ZERO ASSOLUTO.
CENNI SULLE TECNICHE DEL FREDDO E SULLA STORIA DEL RAGGIUNGIMENTO DELLE BASSE TEMPERATURE.
Descrivere, anche per sommi capi, la storia della criochirurgia, implica doverosamente parlare degli scienziati, fisici chimici e ingegneri, che hanno aperto l’attuale via all’uso di strumenti che troviamo nelle sale operatorie come normale dotazione. Il lavoro di questi pionieri ha fornito gli attrezzi che i chirurghi utilizzano per i loro interventi di criochirurgia.
In questa breve rassegna non saranno citati alcuni scienziati mentre altri saranno ricordati per le loro ricerche e scoperte. Questa scelta è, naturalmente, mia responsabilità e per il lettore che desidera approfondire l’argomento rimandiamo a pubblicazioni più aggiornate e meglio dettagliate.
Colgo pertanto l’occasione di ringraziare il dottor Roberto Renzetti che nei suoi articoli La fisica delle basse temperature (parte I e parte II) ha saputo descrivere l’evolversi degli eventi con grande capacità sia descrittiva sia scientifica.
Nella presente bibliografia allegheremo i riferimenti necessari a mettere in contatto il lettore interessato agli articoli da cui abbiamo attinto.
La nostra attenzione si soffermerà sulla figura del prof Linde. Egli è stato, a nostro parere, l’ingegnere che ha reso industriale e quindi commerciale la produzione di gas criogenici. In particolar modo l’azoto liquido che, come sappiamo, è il fluido in uso nella moderna criochirurgia.
Iniziamo, perciò, la nostra indagine storica.
Per rendere più comprensibile cosa sia un ciclo termodinamico criogenico (per abbassare la temperatura a un determinato oggetto) riteniamo utile parlare del ciclo di Carnot che per ragioni strettamente termodinamiche è ritenuto quello di massimo rendimento. E’ pertanto una prestazione teorica cui tutti gli altri cicli si avvicinano, tendono a essa, ma non possono superare.
Per il nostro lavoro può essere superfluo (o comunque non indispensabile) questo capitolo. Lasciamo a scelta del lettore la sua lettura.
Ciclo frigorifero. Ciclo di Carnot
E' un ciclo termodinamico impiegato in modo da sottrarre calore a un corpo che si debba portare e mantenere a temperatura inferiore a quella ambientale. Molto spesso si tratta di spazi entro i quali sono posti i corpi da raffreddare, oppure si tratta di ottenere i corpi in uno stato particolare come ghiaccio dall'acqua, aria e altri gas allo stato liquido, anidride carbonica solida (o ghiaccio secco).
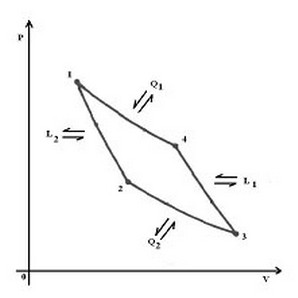
Percorrendo il ciclo 1-4-3-2 si hanno le seguenti operazioni: 1-4 espansione isoterma; 4-3, espansione adiabatica; 3-2 compressione isoterma; 2-1, compressione adiabatica.
Gli scambi energetici con l'esterno sono, in ordine: fornitura di calore Q 1, ottenimento di lavoro L 1, sottrazione di calore Q 2; fornitura di lavoro L 2.
E' noto che il lavoro utile è dato dall'area del ciclo ossia da:
L = L 1 - L 2 = Q 1 - Q 2 e che il rendimento è:
h = L / Q 1 = (Q 1 - Q 2)/ Q 2 = 1- Q 2/Q 1
Il ciclo frigorifero è ottenuto percorrendo la sequenza nel senso opposto 1-2-3-4, ossia sostituendo alle espansioni le compressioni e viceversa. Gli scambi energetici sono, in ordine: ottenimento di lavoro L 2, somministrazione di calore Q 2, fornitura di lavoro L 1, sottrazione di calore Q 1.
Il fabbisogno di lavoro L è posto in evidenza dall'effetto frigorifero:
e = Q 2/L = T 2/(T 1 – T 2)
ossia a parità di temperatura T 2 è tanto maggiore quanto minore è la differenza (T 1 - T 2) e viceversa. Da ciò scaturisce il principio fondamentale della tecnica frigorifera:
il freddo costa tanto più caro quanto
minore è la temperatura T 2, alla quale
lo si vuole ottenere.
In pratica, poiché gli scambi termici esigono scambiatori di calore, le temperature T 1 e T 2 saranno rispettivamente maggiore e minore di quelle teoriche, pertanto l'effetto frigorifero sarà minore, ossia il lavoro speso maggiore di quelli teorici.
L'energia addizionale può essere fornita anche in modo diverso dal lavoro meccanico. Si distinguono pertanto nella tecnica due diversi tipi di processi:
1) quelli che impiegano energia meccanica, in tutte le macchine a compressione;
2) quelli che impiegano energia termica, in tutte le macchine ad assorbimento e a termocompressione.
Il ciclo di Carnot appartiene al primo tipo. In esso però sono previste due trasformazioni isoterme, mentre in realtà il corpo che cede il calore Q 2 si raffredda e quello che riceve il calore Q 1 si riscalda.
Com’è ben noto il ciclo di Carnot è per sua natura ideale: le diverse sequenze studiate e applicate in pratica tendono ad avvicinarsi a esso.
Ricerche europee sulle basse temperature (tra la metà dell’800 ed i primi anni del 900).
In quegli anni Van der Waals scrive l’equazione dei gas (che porta il suo nome). Quest’equazione la cui funzione consiste nell’avvicinare la rappresentazione teorica dei gas alla realtà fisica; fu d’immensa utilità per comprendere il comportamento dei gas reali. La dimensione delle molecole e le forze intramolecolari sono i principali fattori correttivi all’equazione teorica dei gas. Queste modifiche hanno potuto spiegarne i fenomeni concernenti l’espansione.
Regnault nei suoi studi sulla dilatazione dei gas per effetto della temperatura, siamo negli anni 1847, aveva determinato in 1/273 il coefficiente di dilatazione dell’aria (per ogni grado centigrado di temperatura fornito), che andava a migliorare quello determinato prima da Gay-Lussac stimato in 1/266.
Significa che diminuendo di un grado centigrado la temperatura di un gas questi diminuisce di 1/273 di volume. Si deduce che a -273°C il volume di ogni gas dovrebbe essere nullo.
Queste, in parole povere, sono le ragioni per cui la temperatura di -273°C è detta "zero assoluto". E’, in realtà un limite invalicabile per evidenti ragioni volumetriche.
In definitiva secondo i calcoli di Regnault l’aria doveva raffreddarsi un poco quando uscendo da un foro capillare, si espandeva senza fare lavoro.
Fu pertanto Thomson che, servendosi della grande esperienza sperimentale di Joule in una collaborazione durata sette anni, portò alla determinazione che quando le molecole si separano per effetto dell’espansione, occorre un lavoro meccanico per vincere la piccola forza di attrazione che le tiene legate e ciò comporta un assorbimento di calore e quindi un raffreddamento. Questo è l’effetto Joule-Thomson che è fondamentale per la liquefazione dell’aria (vedi in seguito macchina di Linde).
La macchina che sfrutta l’effetto Joule-Thomson è costruttivamente molto più semplice, anche se fornisce in genere un effetto molto piccolo. Si tratta in definitiva di sostituire al motore a espansione il rubinetto di Joule-Thomson.
Furono fatti due brevetti molto simili nel 1985 in Germania per opera di Linde e in Gran Bretagna in nome di Hampson.
Alla fine dell’Ottocento l’evoluzione scientifica incomincia ad avere appoggi della grande industria. Cambia, naturalmente, l’approccio pioneristico che ha caratterizzato l’inizio dell’Ottocento e di pari passo con gli studi teorici sulla comprensione della struttura della materia e della termodinamica s’intraprenderà la strada verso lo zero assoluto.
LINDE
Il professor Dott Carl Paul Gottfried von Linde nacque a Berndorf (Franconia) l’11 giugno del 1842 e morì a Monaco di Baviera il 16 novembre del 1934 all’età di novantadue anni. Studiò e realizzò tecniche di refrigerazione e tecnologie di separazione dei gas.
Linde era un membro di associazioni ingegneristiche e scientifiche, era anche un eminente amministratore dell’Istituto nazionale tedesco di metereologia e dell'accademia bavarese delle scienze e degli studi umanistici. Nel 1861, diciannovenne, Linde s’iscrive a un corso d’ingegneria all’ Istituto di tecnologia federale svizzero a Zurigo. Tra i suoi insegnanti ricordiamo Rudolf Clausius , Gustav Zeuner e Franz Reuleaux.
Nel 1861, diciannovenne, Linde s’iscrive a un corso d’ingegneria all’ Istituto di tecnologia federale svizzero a Zurigo. Tra i suoi insegnanti ricordiamo Rudolf Clausius , Gustav Zeuner e Franz Reuleaux.
Si laurea con successo all'inizio del 1864.
Ha cominciato nello stesso anno come apprendista in una società di filatura di Kottern in Kempten ma è rimasto soltanto per un breve periodo prima di muoversi. Inizialmente verso Borsig a Berlino e poi verso la nuova fabbrica di locomotive del Krauss a Monaco di Baviera, in cui ha lavorato come capo del reparto tecnico.
Nel settembre del 1866 ha sposato Von Helene; la loro unione è durata cinquantatré anni ed hanno avuto sei bambini.
Nel 1868 ha sentito parlare dell'apertura di una nuova Università a Monaco di Baviera ( Technische Hochschule) ed ha fatto immediatamente domanda per un lavoro come conferenziere.
La sua richiesta è stata immediatamente accettata e, data la sua giovane età (aveva soltanto ventisei anni), questo fu un chiaro segnale di quello che diverrà nel futuro la sua carriera.
Linde nel 1870 e 1871 ha pubblicato gli articoli in Industria bavarese e giornale commerciale descrivendo i suoi risultati di ricerca riguardo alla refrigerazione. I primi impianti frigoriferi progettati da Linde ottennero un grande successo commerciale.
Nell’anno 1872 è diventato professore d’ingegneria meccanica. Ha potuto installare un efficiente laboratorio nel quale, tra i suoi allievi, hanno lavorato Diesel von Rudolf (il creatore del famoso ciclo termodinamico e dell’omonimo motore a combustione interna).
Negli anni 1880 Linde si dedica a costruire e vendere le sue macchine per il freddo e, malgrado momenti non proprio favorevoli per il commercio, agli inizi degli anni 1890 la nuova efficiente tecnologia di refrigerazione offre grandi benefici alle fabbriche di birra: aveva venduto 747 macchine. Non solo le fabbriche di birra ma la nuova tecnologia ha trovato successo nei mattatoi e nelle industrie conserviere di tutta Europa.
Nel 1890, Linde, si è spostato di nuovo a Monaco di Baviera in cui ha preso il suo professorship. Nel 1894 ha iniziato un lavoro su un procedimento per la liquefazione dell’aria. Nel 1901, Linde ha iniziato la costruzione di una macchina per ottenere l'ossigeno puro e l'azoto basati sulla distillazione frazionata di aria liquefatta. Dal 1910 insieme al figlio Carl Friedrich sviluppò un processo detto Doppia-colonna di Linde , le cui varianti sono ancora d'uso comune.
Dopo una decade Linde si ritirò dalle attività direttive per dedicarsi alla ricerca e nei primi dieci anni del 1900 riuscì a liquefare l’aria. Comprimendola e quindi lasciandola espandere velocemente, facendole subire in seguito un raffreddamento. Ha ottenuto in tal modo l'ossigeno e l'azoto dall'aria liquida sottoponendola a un lento riscaldamento (distillazione frazionata). L’utilizzo dell'ossigeno trovava grande impiego nella torcia ossiacetilenica, inventata in Francia nel 1904, che ha rivoluzionato il taglio e la saldatura dei metalli nella costruzione delle navi, dei grattacieli e di altre strutture d'acciaio.
Linde, come abbiamo visto, non era solo un rinomato tecnico e un abile ingegnere, era anche un imprenditore eccezionale. Ha formato molte società di successo in Germania e internazionali, lavorando efficacemente per sfruttare al massimo il potenziale dei suoi brevetti. Linde ha, inoltre, fondato la Linde Air Products Company negli S.U.A. nel 1907, un'azienda a che ha i controlli statali degli Stati Uniti negli anni 1940 quella che oggi è chiamata lt Praxair.
Negli anni intorno al 1910 ha iniziato a trasferire le responsabilità dell’azienda ai suoi figli Friedrich e Richard e al suo genero Rudolf Wucherer.
Carl von Linde è morto (come abbiamo detto sopra) a Monaco di Baviera nel novembre 1934 all'età di novantadue anni. Il suo apparecchio per la liquefazione dell’aria ha utilizzato l'effetto di raffreddamento dovuto da un gas compresso che si espande ( Effetto di Joule-Thomson ) con una tecnica di scambio termico in controcorrente che utilizza l'aria fredda prodotta per raffreddare quella ambientale che entra nell'apparecchio. Avremo modo di evidenziare il contributo che la macchina di Linde ha dato per la liquefazione del gas elio e il raggiungimento delle prossimità termiche dello zero assoluto.
Il suo apparecchio per la liquefazione dell’aria ha utilizzato l'effetto di raffreddamento dovuto da un gas compresso che si espande ( Effetto di Joule-Thomson ) con una tecnica di scambio termico in controcorrente che utilizza l'aria fredda prodotta per raffreddare quella ambientale che entra nell'apparecchio. Avremo modo di evidenziare il contributo che la macchina di Linde ha dato per la liquefazione del gas elio e il raggiungimento delle prossimità termiche dello zero assoluto.
L’Europa centro di ricerche mondiali sulle bassissime temperature.
James Dewar (1842-1923), professore di chimica a Cambridge, nel 1878 tenne una lezione alla Royal Institution di Londra. Era solito presentare il venerdì gli esperimenti e le novità scientifiche. Quell’anno informò riguardo alle ricerche di Cailletet e Pictet, servendosi di una loro macchina criogenica giunta da Parigi come regalo del mecenate Warren de la Rue.
Dewar non dava dettagli costruttivi degli apparati che descriveva. Quest’atto aveva come conseguenza due fatti importanti e, precisamente, si dovevano produrre gas liquidi in quantità moderatamente abbondanti e detti gas dovevano essere conservati per un tempo ragionevolmente lungo in modo da permetterne a un pubblico numeroso la verifica.
Nel 1884 nacque la necessità di costruire un proprio laboratorio per creare quell’indipendenza che un’università richiedeva.
Dewar realizzò lo strumento che ancora oggi è in uso e porta il suo nome, il vaso Dewar (noto anche come thermos o criostato). L'obiettivo di Dewar era però quello di liquefare l'idrogeno (e quindi di mostrarlo) ma da alcuni conti sui calori latenti di evaporazione risultava che i sistemi d’isolamento di Cailletet non avrebbero permesso di mantenere l'idrogeno liquido. Nel 1892, apportò le modifiche che lo misero in grado di contenere e mantenere l'idrogeno liquido e mostrò il suo apparato in una forma definitiva in una conferenza del gennaio del 1893. La novità delle esperienze di questi anni, rispetto a ciò che si aveva, è l'uso del vuoto come isolante molto migliore dell'aria che prima c'era nell'intercapedine.
Si serviva di una macchina che utilizzava l'effetto Joule-Thomson.
Ricordiamo che detto apparato era già utilizzato da Linde e che proprio grazie allo scienziato tedesco l’apporto al progresso delle scienze criogeniche non deve essere dimenticato.
Descriviamo, utilizzando uno schema sintetico, il funzionamento di detta macchina di Linde (o Hampson).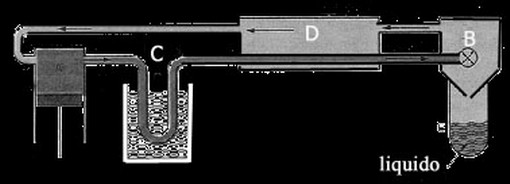
Il fluido evolvente cicla nella macchina passando a condizioni fisiche successive. Nel recipiente A è compresso e, dopo aver attraversato un condensatore C, arriva a uno scambiatore di calore D di qui al recipiente B nel quale è soggetto a un’espansione attraverso un beccuccio. In questo processo si ottiene un lieve abbassamento di temperatura in modo che il gas che si espande, in D, raffredda quello in arrivo.
In questo ciclo vi è un continuo e progressivo abbassamento di temperatura nel fluido finché questi inizia a liquefare raccocliendosi in E.
Dewar aveva la sensazione di essere prossimo alla meta. Il 9 luglio giunse da Leida la notizia che distrusse ogni sua speranza: l’elio è stato liquefatto dal professore dott K amerling Onnes, presso l’Università di Leida, il 9 luglio 1908.
Dewar non era certo un animo sereno e gentile, abbandonò le ricerche sulla criotecnica e divenne sempre più litigioso e ombroso. Condusse una vita ritirata. Così, perdendo un valido professore, la Gran Bretagna non fece più ricerche sulle basse temperature.
KAMERLINGH ONNES A LEIDA.
Nacque a Graminga il 21 settembre del 1853 e morì a Leida il 21 febbraio del 1926.
Era un ottimo fisico sperimentale che non disdegnava però gli approcci teorici.
Era una persona di animo gentile e molto paziente che faceva della precisione uno dei suoi riferimenti importanti, tanto che inaugurò il suo corso di fisica con una lezione che aveva per titolo proprio L'importanza della ricerca quantitativa nella fisica. Egli attrezzò il suo laboratorio in modo che fosse funzionale orientato a ricerche di elevatissima precisione tanto che, a parte i suoi successi personali, quei laboratori furono esempio per la costruzione di vari altri in diverse parti del mondo.
Lavorò in stretto contatto con l’industria. Nel suo laboratorio si soffiava il vetro e si realizzavano strumenti di precisione; si stampava una rivista scientifica, Comunicazioni del Laboratorio di Fisica dell'Università di Leida, che aggiornava in modo comprensibile su ogni passo che si percorreva sulla strada delle basse temperature e che divenne uno strumento indispensabile per ogni laboratorio di ricerca che si occupasse dei medesimi problemi.
L'elio, estratto da alcune sabbie di monazite, gli veniva nel frattempo procurato in quantità importanti tramite l'interessamento di suo fratello che dirigeva l'Ufficio delle Informazioni Commerciali. Come scriveva Kamerlingh Onnes, la preparazione di elio puro in grandi quantità divenne principalmente una questione di perseveranza e cura. Intanto le officine meccaniche avevano disponibile il progetto della macchina che avrebbe dovuto liquefare l'elio. Si trattava di un grande impianto basato sulla macchina ciclica di Linde che fu pronto a operare nel giugno del 1908.
Fu proprio Onnes a indirizzare la sua ricerca sulle proprietà della materia a quelle temperature. Una delle ricerche che per prima fu realizzata dal 1911 riguardava quell'anomalia della resistenza e della resistività dei conduttori che sembravano diminuire quando la temperatura scendeva fino ad annullarsi allo zero assoluto (questo fu un problema per Onnes che gli impedì di utilizzare i termometri funzionanti con le variazioni della resistenza di certi metalli) e, con gli sviluppi commerciali dell'elettricità, la cosa fu d’interesse industriale e generale. Il problema della resistenza alle basse temperature se l'era posto anche Dewar ma aveva complicato i problemi più che risolverli.
Il chimico fisico Walther Nerst (1864-1941) formulava l'ipotesi che all'approssimarsi allo zero assoluto, la resistenza doveva annullarsi.
Kamerlingh Onnes si mise a ricercare proprio da lì, dalle temperature alle quali Dewar aveva lasciato e, con il suo metodo preciso e rigoroso, pubblicò una serie di memorie sulle misure sperimentali realizzate sulla resistività di vari metalli a bassissime temperature. Anche qui sorsero varie difficoltà nelle prime esperienze perché sembrava che quando la temperatura diminuiva la resistenza si mantenesse costante. Si era in uno stallo completo senza poter sostenere l'una o l'altra teoria e/o misura. Vi fu però un'osservazione risolutiva dello stesso Onnes sui campioni di metallo che utilizzava. Dato uno stesso tipo di metallo, la resistenza (indipendentemente dal variare dalla temperatura) variava da campione a campione ed era minore quanto più puro era il metallo. Ciò poteva solo dipendere dalle impurità contenute nel campione e Onnes si spostò su questa linea di ricerca. Scelse quindi i metalli che, con le tecnologie dell'epoca, si potevano meglio purificare iniziando dall'oro che era migliore del platino sotto questo profilo. L'esperienza con l'oro andava nel senso di quanto sostenuto da Nerst, la resistività diminuiva al diminuire della temperatura. Con una profonda differenza però che Onnes non colse subito perché le sue idee, sulla linea di Nerst, furono un pregiudizio. Ora affermare con Nerst che allo zero assoluto la resistività diventa nulla rimarrebbe, se il fatto fosse confermato, nell'ambito dell’inutilità della cosa, viste le difficoltà per arrivare a qualche grado sopra tale zero. Cercare però ciò che stava trovando Onnes, che la resistività si annullava alle temperature agibili con l'elio liquido, era un fenomeno dalle caratteristiche profondamente differenti. In ogni caso Onnes fornì una formula del comportamento della resistività nel caso dell'oro che prevedeva una resistività che andava a zero con lo zero assoluto. E qui è utile dare un riferimento alla fisica teorica che era reclamata, anche se in modo piuttosto pasticciato. Per spiegare la considerevole diminuzione di resistenza, virtualmente a zero, ai 4,2°K e il fatto che la resistenza resterebbe a zero per temperature inferiori, Onnes si servì della teoria dei quanti di Planck.
Utilizzando gli oscillatori della teoria dei calori specifici di Einstein e un miscuglio di Planck, Einstein e teoria degli elettroni di Lorentz, Onnes presentò la sua formula della conducibilità elettrica in funzione della temperatura. A basse temperature non erano gli elettroni ma gli oscillatori che tendevano a congelare, in funzione delle loro frequenze ricavabili dai calori specifici.
Onnes stette un intero anno a lavorare sul mercurio per capire gli strani fenomeni che aveva notato e della cui esistenza dava un solo cenno in chiusura della memoria del novembre 1911. Rileggiamo Onnes nel 1913 in tre successive e lunghe memorie del febbraio, marzo e maggio. Studiava le proprietà di altri materiali alle basse temperature anche per scoprire la validità della legge di Ohm. Si convinse che esiste un punto di transizione di sotto al quale tale legge non ha più valore e introdusse (nella memoria del marzo) il termine superconduttività K. Onnes non riuscì mai a solidificare l'elio. La comprensione del problema avvenne solo dopo la sua morte che avvenne nel 1926 dopo che ebbe il Nobel per la fisica nel 1913 (per la sua scoperta della superconduttività del 1911).
Onnes ricevette il Premio Nobel per la fisica all’età di 60 anni.  Kamerlingh Onnes, oltre i suoi impegni scientifici, era un uomo dedito alla famiglia ed era sempre e comunque disponibile nei riguardi di coloro che ne avevano bisogno. Possedeva un grande fascino personale ed aveva un’umanità filantropica. E’ stato molto attivo durante e dopo la prima guerra mondiale diffondendo la comprensione delle differenze politiche tra gli scienziati e soccorrendo i bambini che muoiono di fame in paesi che soffrono di scarsità di cibo.
Kamerlingh Onnes, oltre i suoi impegni scientifici, era un uomo dedito alla famiglia ed era sempre e comunque disponibile nei riguardi di coloro che ne avevano bisogno. Possedeva un grande fascino personale ed aveva un’umanità filantropica. E’ stato molto attivo durante e dopo la prima guerra mondiale diffondendo la comprensione delle differenze politiche tra gli scienziati e soccorrendo i bambini che muoiono di fame in paesi che soffrono di scarsità di cibo.
Nel 1887 si sposò con Maria Adriana Wilhelmina Elisabeth Bijleveld, che fu per lui un grande aiuto in queste attività e che seppe creare nella sua casa un centro molto conosciuto per l’ospitalità e la cultura. Hanno avuto un figlio, Alberto, che divenne un alto funzionario nella capitale L’Aia.
Kamerlingh Onnes ha sempre avuto una salute cagionevole e, dopo una breve malattia, si è spento a a Leida il 21 febbraio 1926.
Con lui l’Umanità perde un grande uomo nel più ampio e profondo senso della parola.
Siamo giunti alla parte conclusiva del nostro modesto lavoro che, per passi successivi, cerca di evidenziare gli sforzi dei ricercatori per comprendere le leggi che governano i gas a temperature prossime allo zero assoluto.
Abbiamo costatato che studiosi francesi, olandesi, inglesi, polacchi, tedeschi e altri hanno contribuito al progresso di questa scienza. E così deve essere. E’ vero che la fisica è appannaggio di pochi uomini ma il patrimonio culturale che da essa scaturisce fa parte dell’umanità.
E, forse, in questo consiste la vera forza delle scienze come reale appannaggio dell’uomo perché tale.

